Cho m g hỗn hợp X gồm NaBr và CaCl2 vào đ AgNO3 dư, sau phản ứng thu được 2m g kết tủa (gồm AgBr và AgCl) . Tính % khối lượng mỗi kim loại trong hỗn hợp X.

Những câu hỏi liên quan
hỗn hợp gồm NaCl và NaBr tác dụng với dd AgNO3 dư thu được hỗn hợp hết tủa(AgCl và AgBr) có k/lg bằng k/lg AgNO3 đã dùng. tính phần trăm mỗi muối trong hỗn hợp ban đầu
Gọi nNaCl = x mol; nNaBr = y mol
NaCl + AgNO3 → NaNO3 + AgCl
NaBr + AgNO3 → NaNO3 + AgBr
Vì khối lượng kết tủa bằng khối lượng AgNO3 phản ứng
=> 170.(x + y) = 143,5x + 188y
=> 26,5x = 18y
=> \(y=\dfrac{53}{36}x\)
=> \(\%m_{NaCl}=\dfrac{58,5x}{58,5x+103y}.100=\dfrac{58,5x}{58,5x+103.\dfrac{53}{36}x}.100=27,84\%\)
=> %mNaBr = 100- 27,84 = 72,16%
Đúng 2
Bình luận (0)
cho 19,3 g hỗn hợp bột A gồm Zn và Cu vào 400 ml dd AgNO3 1M. Sau khi phản ứng xong được 49,6 g hỗn hợp 2 kim loại và dung dịch B. Thêm một lượng dư dung dịch KOH vào dung dịch B được kết tủa. Lọc lấy kết tủa đem nung đến khối lượng không đổi được m gam chất rắn. Viết phương trình phản ứng hóa học của các phản ứng xảy ra và tính giá trị của m
Hỗn hợp 2 KL gồm: Ag và Cu dư.
PT: \(Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\)
\(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
\(Zn\left(NO_3\right)_2+2KOH\rightarrow2KNO_3+Zn\left(OH\right)_2\)
\(Cu\left(NO_3\right)_2+2KOH\rightarrow2KNO_3+Cu\left(OH\right)_2\)
\(Zn\left(OH\right)_2+2KOH\rightarrow K_2ZnO_2+2H_2O\)
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
Chất rắn thu được sau pư là CuO.
Ta có: \(n_{AgNO_3}=0,4.1=0,4\left(mol\right)\)
Theo PT: \(n_{Ag}=n_{AgNO_3}=0,4\left(mol\right)\)
Mà: mAg + mCu dư = 49,6 (g)
⇒ mCu (dư) = 49,6 - 0,4.108 = 6,4 (g)
Ta có: 65nZn + 64nCu (pư) = 19,3 - 6,4 (1)
Theo PT: \(n_{AgNO_3}=2n_{Zn}+2n_{Cu\left(pư\right)}=0,4\left(2\right)\)
Từ (1) và (2) ⇒ nZn = nCu (pư) = 0,1 (mol)
Theo PT: \(n_{CuO}=n_{Cu\left(OH\right)_2}=n_{Cu\left(NO_3\right)_2}=n_{Cu\left(pư\right)}=0,1\left(mol\right)\)
⇒ m = mCuO = 0,1.80 = 8 (g)
Đúng 3
Bình luận (0)
A là dung dịch AgNO3 nồng độ a M . cho 13.8 g hỗn hợp sắt và đồng vào 750 ml dung dịch A , sau phản ứng kết thúc thu được dung dịch B và 37.2 g chất rắn E . Cho NaOH dư vào dung dịch B thu được kết tủa . Lấy kết tủa nung đến trong không khí đến khối lượng không đổi thu được 12g hỗn hợp 2 oxit của 2 kim loại .
a) Tính % theo khối lượng mỗi kim loạib) Tính a=?
câu a2AgNO32x+Fex⟶Fe(NO3)2x+2Ag2x2AgNO32x+Fex⟶Fe(NO3)2x+2Ag2x2AgNO32y+Cuy⟶Cu(NO3)2y+2Ag2y2AgNO32y+Cuy⟶Cu(NO3)2y+2Ag2y ⇒m⇒mchất rắn tăng=mAg−mFe+mAg−mCu=mAg−mFe+mAg−mCu⇔37,2−13,8=216x−56x+216y−64y⇔37,2−13,8=216x−56x+216y−64y⇔160x+152y=23,4(1)⇔160x+152y=23,4(1) 2Fe(NO3)2 2Fe(OH)2 Fe2O3 x x 0,5x => => Cu(NO3)2 Cu(OH)2 CuO y y y => 160.0,5x + 80y = 12 (2) (1) và (2) => x= 0,075 y=0,075=> %Fe = 46,67% %Cu=53,33%câu bnAgNO3 pư= 2x+2y = 0,3 mol=> a= 0,3/ 0,75= 0,4M
Đúng 2
Bình luận (0)
Cho 12,4 g hỗn hợp x gồm 2 kim loại cu và mg vào dung dịch H2SO4 loãng dư,thu được 5,6 lít khí(đktc) A)Tính khối lượng mỗi kim loại trong hỗn hợp x B)Cho hỗn hợp trên tác dụng với dung dịch AgNO3 dư tính khối lượng kim loại tạo thành Giải giúp ghi rõ a)b)c) để mình biết
Cho hỗn hợp X gồm Al, Fe vào dung dịch chứa AgNO3 và Cu(NO3)2. Sau phản ứng thu được hỗn hợp Y gồm 2 kim loại và dung dịch Z. Cho NaOH dư vào dung dịch Z thu được 2 kết tủa gồm 2 hiđroxit kim loại. Xác định các chất trong hỗn hợp Y và dung dịch Z. Viết các phương trình phản ứng xảy ra
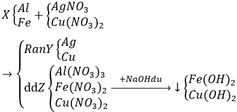
Pt:
Al + 3AgNO3 → Al(NO3)3 + 3Ag↓
2Al + 3Cu(NO3)2 → 2Al(NO3)2 + 3Cu↓
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag↓
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu↓
Al(NO3)3 + 3NaOH → Al(OH)3↓ + 3NaNO3
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Fe(NO3)2 + 2NaOH → Fe(OH)2↓ + 2NaNO3
Cu(NO3)2 + 2NaOH → Cu(OH)2↓ + 2NaNO3
Đúng 0
Bình luận (0)
Đốt cháy 22,2 gam hỗn hợp gồm AL và Fe trong khí Br2 dư . Sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp X . Cho Xtác dụng với dung dịch KOH dư thu được kết tủa , đêm nung kết tủa trong kk đến khối lượng ko đổi được 24 g rắn . % khối lượng mỗi kim loại trong hỗn hợp là ?
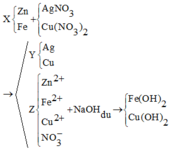
Cho hỗn hợp X gồm Zn, Fe vào dung dịch chứa AgNO3 và Cu(NO3)2, sau phản ứng thu được hỗn hợp Y gồm 2 kim loại và dung dịch Z. Cho NaOH dư vào dung dịch Z thu được kết tủa gồm hai hiđroxit kim loại. Dung dịch Z chứa? A. Zn(NO3)2, AgNO3, Fe(NO3)3 B. Zn(NO3)2, Fe(NO3)2 C. Zn(NO3)2, Fe(NO3)2, Cu(NO3)2 D. Zn(NO3)2, Cu(NO3)2, Fe(NO3)3
Đọc tiếp
Cho hỗn hợp X gồm Zn, Fe vào dung dịch chứa AgNO3 và Cu(NO3)2, sau phản ứng thu được hỗn hợp Y gồm 2 kim loại và dung dịch Z. Cho NaOH dư vào dung dịch Z thu được kết tủa gồm hai hiđroxit kim loại. Dung dịch Z chứa?
A. Zn(NO3)2, AgNO3, Fe(NO3)3
B. Zn(NO3)2, Fe(NO3)2
C. Zn(NO3)2, Fe(NO3)2, Cu(NO3)2
D. Zn(NO3)2, Cu(NO3)2, Fe(NO3)3
Cho hỗn X gồm Zn, Fe vào dung dịch chứa
A
g
N
O
3
và
C
u
N
O
3
2
, sau phản ứng thu được hỗn hợp Y gồm 2 kim loại và dung dịch Z. Cho NaOH dư vào dung dịch Z thu được kết tủa gồm 2 hiđroxit kim loại. Dung dịch Z chứa A.
Z
n...
Đọc tiếp
Cho hỗn X gồm Zn, Fe vào dung dịch chứa A g N O 3 và C u N O 3 2 , sau phản ứng thu được hỗn hợp Y gồm 2 kim loại và dung dịch Z. Cho NaOH dư vào dung dịch Z thu được kết tủa gồm 2 hiđroxit kim loại. Dung dịch Z chứa
A. Z n N O 3 2 , C u N O 3 2 , F e N O 3 3
B. Z n N O 3 2 , C u N O 3 2 , F e N O 3 2
C. C u N O 3 2 , F e N O 3 2
D. Z n N O 3 2 , A g N O 3 , F e N O 3 2
Hỗn hợp X gồm M2CO3, MHCO3 và MCl với M là kim loại kiềm. Nung nóng 20,29 gam hỗn hợp X, sau khi phản ứng xảy ra hoàn toàn thấy còn lại 18,74 g chất rắn. Nếu lấy 20,29 g hỗn hợp X trên tác dụng hết với 500 ml dung dịch HCl 1M thì thoát ra 3,36 lít khí (đktc) và thu được dung dịch Y. Cho Y tác dụng với dung dịch AgNO3 dư thì thu được 74,62 g kết tủa. Phần trăm khối lượng của kim loại M trong MCl gần đúng với A. 39% B. 16% C. 70% D. 52%
Đọc tiếp
Hỗn hợp X gồm M2CO3, MHCO3 và MCl với M là kim loại kiềm. Nung nóng 20,29 gam hỗn hợp X, sau khi phản ứng xảy ra hoàn toàn thấy còn lại 18,74 g chất rắn. Nếu lấy 20,29 g hỗn hợp X trên tác dụng hết với 500 ml dung dịch HCl 1M thì thoát ra 3,36 lít khí (đktc) và thu được dung dịch Y. Cho Y tác dụng với dung dịch AgNO3 dư thì thu được 74,62 g kết tủa. Phần trăm khối lượng của kim loại M trong MCl gần đúng với
A. 39%
B. 16%
C. 70%
D. 52%
Đáp án C
Đặt số mol của M2CO3, MHCO3, MCl là x,y,z mol
Đun nóng X :
2MHCO3 → M2CO3 + H2O + CO2
mrắn giảm = 18. y/ 2 + 44.y/2 =20,29 -18,74 → y = 0,05 mol
X tác dụng với 0,5 mol HCl :
M2CO3 + 2HCl → 2MCl + H2O + CO2
MHCO3 + HCl → MCl + H2O + CO2
nCO2 = x + y = 0,15 → x =0,1mol → nHCl phản ứng = 2.0,1 + 0,05 =0,25 mol < nHCl ban đầu
→ HCl dư
Dd Y có MCl và có thể có HCl dư
Ag+ + Cl- → AgCl
0,52 mol
→ nCl- = 0,52 = nHCl + nMCl (ban đầu) = 0,5 + z → z = 0,02 mol
Ta có mX = 0,1 (2M + 60) + 0,05 ( M + 61) + 0,02 (M + 35,5) → M = 39 (K)
Trong KCl thì %K = 39/74,5 .100% =52,35 %
Đúng 0
Bình luận (0)